온라인으로 영역 넓힌 제약사 영업망…해외까지 진출
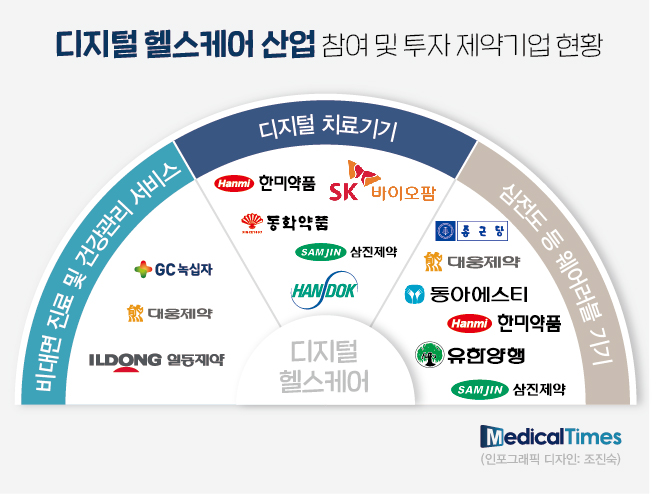
메디칼타임즈=문성호 기자코로나 대유행 장기화 여파로 시작된 제약사들의 의사 대상 '온라인 플랫폼' 구축 열풍.올해 코로나가 풍토병화 되는 엔데믹 시대에 본격 접어들면서 구축했던 '온라인 플랫폼' 활용 방안 마련이 제약사들의 화두로 떠올랐다. 대면 영업‧마케팅 활동이 본격 재개된 데에 따른 영향이다.이 가운데 최근 동아에스티가 온라인 플랫폼 활용 방안이 주목받고 있다.동아에스티가 자사 온라인 플랫폼 '메디플릭스'를 활용해 학술강좌를 진행하는 모습이다. KT와 손잡고 동아에스티는 관련 학술 콘텐츠를 베트남 의료진에 교육자료로 활용한다는 방침이다.22일 제약업계에 따르면, 최근 동아에스티는 KT와 자사 의료지식 공유 플랫폼 '메디플릭스(Mediflix)'를 활용한 베트남 의료교육 업무협약을 체결했다.협약에 따라 동아에스티는 KT의 의료교육 플랫폼에 동아에스티의 의료지식 공유 플랫폼 '메디플릭스(Mediflix)'의 의료지식 콘텐츠를 제공하고, KT의 신규 자체 콘텐츠 제작을 지원한다.기존 국내 의료진 대상 학술적 내용을 전달하는 것에 더해 베트남 의료진 대상으로도 '메디플릭스'가 의료정보를 전달하게 되는 매개체로 활용되는 것이다.코로나 엔데믹 전환에 따른 대면 영업‧마케팅 활동이 재개됨에 따라 각 제약사 별 온라인 플랫폼 활용도가 감소되는 시기 새로운 활용 방안을 마련했다는 점에서 주목받고 있다. 동아에스티의 경우 코로나 대유행 시기 자사 온라인 플랫폼이었던 '쇼타임'을 리뉴얼, 현재의 '메디플릭스'로 개편해 재오픈한 바 있다. 이를 통해 온라인 학술대회 개념의 'Korea Disease Week(KDW)'를 제약사 중에선 최초로 개최하는 등 코로나 대유행 시기 온라인 플랫폼을 활용한 영업‧마케팅 방안으로 적극 활용해왔다.특히 동아에스티가 이 같은 온라인 학술대회를 도입하자 국내 상위 제약사를 필두로 잇따라 경쟁적으로 자사 플랫폼을 활용해 유사한 형태 행사를 개최, 영업‧마케팅을 전개하고 있다.하지만 동아에스티는 엔데믹 전환 이후 이 같은 온라인 학술대회 개최를 중단하는 한편, 베트남을 시작으로 해외 의료인을 대상으로 한 의료 콘텐츠 제공이라는 새로운 활용방안을 마련하게 됐다.온라인 플랫폼 활용방안으로 고민 중인 다른 제약사에게도 새로운 활용방안으로서의 모델을 제시했다고 볼 수 있다.따라서 동아에스티는 베트남에서 의료분야 디지털전환(DX, Digital Transformation) 사업을 추진 중인 KT와 손을 잡으며, 현지 의료인 대상으로 메디플릭스를 활용해 국내 의료인들이 진행한 교육 콘텐츠를 제공하겠다는 구상이다.이와 관련해 KT는 베트남에서 원격의료 및 건강검진 등 다양한 헬스케어 사업을 구상 중이다. 이 과정에서 베트남 의료진을 대상으로 한 교육 콘텐츠 제공 과정에서 동아에스티의 메디플릭스를 활용하는 것이다.동아에스티도 최근 디지털 헬스케어 사업에 뛰어드는 과정에서 수익적 관점보다는 저변 확대 차원에서의 메디플릭스의 활용도 증가에 초점을 맞추고 있다.동아에스티 관계자는 "베트남 의료진을 대상으로 국내 선진적인 의료 콘텐츠를 제공하는 데 의미가 있다. KT와 이 같은 교육에 대한 필요성에 공감해 참여하게 됐다"며 "베트남 헬스케어 사업을 추진함과 동시에 사회에 기여하자는 의미에서 메디플릭스를 활용한 교육 콘텐츠 제공"이라고 강조했다.한편, 코로나 대유행 전‧후로 주요 제약사들이 비대면 영업‧마케팅 수단 차원에서 의사 대상 온라인 플랫폼을 경쟁적으로 마련한 바 있다. 현재 제약사 외 기존 의료전문 플랫폼 기업들까지 합하면 30개가 넘어서는 상황이다.